چطور عیار طلا را با اسید نیتریک تشخیص بدهیم؟
جواهرات طلا در آلیاژهای مختلف ساخته می شوند ، از طلای خالص تا وزن کمتر از نصف طلا. طلای خالص را 24 عیار یا 24 K می نامند. 75٪ طلا (از نظر وزنی) 18 K است. و 50٪ طلا 12 K است.
بررسی واکنشهای اسید نیتریک و طلا (استحصال طلا با اسید نیتریک)
طلا غالباً در جواهرات با نقره و مس آلیاژ می شود تا هزینه را کاهش دهد و در برابر سایش سخت تر و مقاوم تر شود. آیا تاکنون فکر کرده اید که جواهرات شما چه طلای عیار است؟ برای تقریب عیار می توانیم از شیمی استفاده کنیم! به منظور بررسی بیشتر کاربرد تیزاب سلطانی و واکنش آن با طلا با ادامه مقاله همراه باشید.
آلیاژهای طلا علیرغم اینکه سخت تر از طلای خالص هستند ، می توانند راحت تر از طلای خالص در اسیدها حل شوند. بنابراین ، هرچه عیار پایین تر باشد ، آلیاژ طلا به راحتی حل می شود.
معادلات زیر را مشاهده کنید ، که نتایج حاصل از افزودن اسید نیتریک غلیظ ، HNO3 یا تیزآب سلطانی(محلولی بسیار خورنده و دودکننده زرد یا قرمز رنگ است. این محلول از مخلوط اسید نیتریک غلیظ و هیدروکلریک اسید غلیظ بدست میآید که معمولاً به نسبت حجمی یک به سه میباشند.)به عیارهای مختلف طلا را نشان می دهد. Aqua regia مخلوطی از اسیدهای نیتریک و هیدروکلریک است. نام خود را از توانایی آن در حل کردن طلا گرفته است که گاهی اوقات به آن تیز آب سلطنتی نیز گفته می شود. "Aqua" کلمه لاتین آب و "regia" لاتین سلطنتی است.
برای خرید هیدروکلریک اسید کلیک کنید
همانطور که در معادله اول مشاهده شد ، یک آلیاژ طلا از 14 K (عیار14) یا کمتر با افزودن اسید نیتریک حل می شود. اما هنگامی که عیار به 18 یا بالاتر می رود (معادله دوم) ، اسید نیتریک هیچ واکنشی قابل مشاهده نمی کند. فقط محلول اسید تیزآب سلطانی می تواند عیارهای بالاتر طلا را حل کند (معادله سوم).
برای فروش اسید نیتریک کلیک کنید
طلای14عیار یا پایینتر + HNO3 (aq) → Cu + یا Ag + (aq) آلیاژ حل می شود
طلای 18عیار یا بالاتر+ HNO3 (aq) → هیچ آلیاژ واکنشی حل نمی شود
تیزآب سلطانی+ طلای 18 عیار یا بالاتر→AuCl4- (aq) آلیاژ حل می شود
در روش زیر برای تعیین عیار نمونه های طلا از اسید نیتریک و تیزآب سلطانی و شاید از سایر راه حل های آزمایش استفاده خواهید کرد. هنگام انجام آزمایشات ، از تصویر زیرمیتوانید استفاده کنید.
مواد مورد استفاده برای استخراج طلا با اسید نیتریک
مواد و راه حل های تست ذکر شده در زیر را می توانید از فروشگاه لوازم طلا و مواد شیمیایی تهیه کنید.
دستکش ، عینک ایمنی و لباس محافظ و ماسک مخصوص آنتی اسید
سنگ محک: یک تخته مسطح بازانیت
نمونه طلا برای آزمایش (ممکن است از جواهرات لباس استفاده شود و دانش آموزان داوطلب شوند تا قطعات خود را آزمایش کنند. لطفا توجه داشته باشید که روکش طلا بر روی جواهرات لباس بسیار نازک است و فشار اضافی به فلز پایه خراشیده می شود)
مجموعه ای از سوزن های آزمایش طلا (اینها استانداردهای طلا آلیاژهای شناخته شده، برای مقایسه نمونه های طلای ناشناخته است. آلیاژهای پیشنهادی: K10 ،14 K ،18 K ،(20 K
قطره چکان
اسید نیتریک (HNO3) ، محلول 65٪
تیزاب سلطانی**
سایر راه حل های آزمایش (اختیاری)
** مواد مورد نیاز برای تهیه تیزاب سلطانی چیست؟
فقط در کار با اسیدها و تهیه این محلول ها باید با کارشناسان با تجربه در ارتباط باشید.
2 ظرف واکنش دهنده ضد اسید
2 سیلندر مدرج
آب دی یونیزه (میتوانید در مقاله تفاوت آب مقطر با آب دی یونیزه اطلاعات بیشتری کسب کنید)
اسید نیتریک (HNO3) ، غلیظ
اسید کلریدریک (HCl) ، غلیظ
توجه: پسماند حاصل از این آزمایش باید قبل از شستشو خنثی شود.
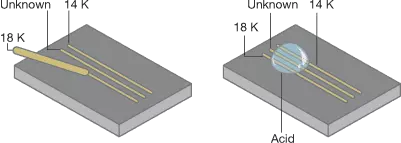
روش آزمایش:
لطفاً قبل از شروع ، کل مراحل را مطالعه کنید.
هشدار: لطفاً حتماً از دستکش ، عینک ایمنی و لباس محافظ استفاده کنید - اسیدهایی که در این فعالیت استفاده خواهید کرد بسیار خورنده و سمی هستند. اگر اسیدهایی به طور تصادفی ریخته شدند ، بی کربنات سدیم خشک را روی محلول اسید بریزید تا خنثی شود. اگر اسیدی با پوست تماس گرفت ، بلافاصله محل را کاملاً با آب بشویید.
- دستکش ، عینک ایمنی و لباس محافظ بر تن کنید
- با نمونه مورد آزمایش ، یک رگه (به طول حدود 2 سانتی متر) بر روی سنگ محک ایجاد کنید.
- با استفاده از همان فشار ، یک رگه از یک طرف (حدود 2 میلی متر از ردیف اول) با یک سوزن آزمایش طلا از عیار پایین تر از آنچه انتظار می رود ، ایجاد کنید. (شما باید حدس بزنید که عیار ناشناخته چه عیاری است !) در طرف دیگر با یک استاندارد طلای شناخته شده از عیار بالاتر از آنچه حدس زدید،رگه ای ایجاد کنید.
- در یک انتهای رگه ها ، با استفاده از قطره چکان ، یک قطره از محلول آزمایش مناسب برای عیار نمونه طلای ناشناخته خود قرار دهید با مراجعه به معادلات سمت چپ ، راه حل مناسب آزمایش را تعیین کنید. به عنوان مثال ، اگر فکر می کنید ناشناخته شما طلای 12 K است ، اسید نیتریک را انتخاب کنید.
- اطمینان حاصل کنید که قطره رگه ها را مانند تصویر نشان داده است. واکنش (واکنش تیزاب سلطانی با طلا) را با دقت مشاهده کنید. احتمالاً خواهید دید که رگه ها از نظر ظاهری سبک تر می شوند و در نهایت ممکن است کاملاً از بین روند. این آلیاژ محلول در اسید است. آلیاژهای طلای عیار پایین کمتر از آلیاژهای بالاتر عیار حل می شوند زیرا حاوی مس یا نقره بیشتری هستند که در اسید نیتریک حل می شوند ، در حالی که طلا اینگونه نیست. به عنوان مثال ، اگر با معیار ناشناخته خود رگه ای از 10 K و 12 K طلای استاندارد ترسیم کرده باشید که به اعتقاد شما 12 K است، رگه از استاندارد طلای 12 K و ناشناخته شما باید با همان سرعت حل شود ، در حالی که 10 K خط استاندارد طلا باید سریعتر حل شود. همچنین ، پس از شستشوی اسید از سنگ محک با آب ، طلای بیشتری در رگه 12 K نسبت به رگه 10 K باقی خواهد ماند.
- اگر تیزآب سلطنتی اعمال شود ، در پایان واکنش هیچ طلایی بر روی سنگ محک باقی نمی ماند. شما با مشاهده دقیق میزان حل شدن رگه ها ، عیار را تعیین خواهید کرد ، در حالی که بالاترین عیار رگه کمترین سرعت در حل شدن را دارد.
- در صورت نیاز ، قطره دیگری از محلول آزمایش دیگر را در انتهای دیگر رگه ها قرار دهید. نتایج را با دقت مشاهده کنید. اگر نتایج مبهم باشد ، ممکن است لازم باشد چندین بار آزمایش را تکرار کنید ، رگه های جدیدی با استانداردهای مختلف طلا ایجاد کنید و از محلول های جایگزین آزمایش اسید استفاده کنید.
لطفا توجه داشته باشید: این آزمون خوب کار می کند ، اما نتایج باید به عنوان یک تقریب تلقی شود. دو نمونه طلای 14 K که حاوی فلزات آلیاژی مختلف هستند (مانند نقره یا مس) در این آزمایش واکنش متفاوتی نشان می دهند. به همین ترتیب ، رگه ضخیم تر و سنگین تر طلای 18 K ممکن است با سرعت کمتری از رگه نازک طلای 20 K حل شود. بنابراین ، مهم است که هر سوزن آزمایش با همان فشار بر روی سنگ ماسه سنگ اعمال شود. برای آلیاژهای کمتر از 10 K ، رگه ها تقریباً بلافاصله در 65٪ اسید نیتریک حل می شوند. برای این آلیاژها ممکن است از اسید نیتریک رقیق (35٪) استفاده شود. به همین ترتیب ، آلیاژهای کمتر از 18 K به سرعت در تیزآب سلطنتی حل می شوند ، به طوری که اختلاف میزان واکنش را نمی توان مشاهده کرد. برای آزمایش این آلیاژها از تیزآب رقیق (50٪) استفاده کنید.
بررسی دقیق تر واکنش های مربوط به فرایند استخراج طلا با نیتریک اسید
این دو محلول آزمایش اسیدی با حل شدن تمام یا برخی از فلزات موجود در آنها ، با آلیاژهای طلا واکنش نشان می دهند. اسید نیتریک مس و نقره را با اکسید کردن آنها حل می کند ، همانطور که در معادلات شیمیایی زیر شرح داده شده است.
اکسیداسیون مس در اسید نیتریک:
Cu (s) + 2 NO3- (aq) + 2 H + (aq) 2 Cu2 + (aq) + 2 NO2 (g) + H2O (l)
اکسیداسیون نقره در اسید نیتریک:
Ag (s) + 2 NO3- (aq) + 2 H + (aq) → Ag + (aq) + 2 NO2 (g) + H2O (l)
هرچه مس یا نقره بیشتر در آلیاژ طلا باشد ، آلیاژ سریعتر حل می شود. آلیاژهای طلا بیشتر از 14 K هنوز با اسید نیتریک واکنش نشان می دهند (جز copper مس یا نقره آلیاژ هنوز حل می شود) ، اما چون مس یا نقره کمتری برای واکنش وجود دارد ، مشاهده واکنش بسیار سخت تر خواهد بود. برای آلیاژهای بیشتر از 14 K ، از تیزآب سلطنتی برای آزمایش طلا استفاده می شود.
در بررسی بیش تر کاربرد تیزاب سلطانی باید گفت که تیزآب سلطنتی خود طلا را حل می کند (و همچنین اجزای نقره و مس را حل می کند) و به همین دلیل برای آزمایش آلیاژهای طلای بالاتر از عیار استفاده می شود. تیزآب سلطنتی طلا را در دو واکنش جداگانه حل می کند. اولین واکنش اکسیداسیون است که توسط اسید نیتریک ایجاد می شود و مقدار کمی طلای محلول و اکسید شده Au3
+ تولید می کند (3). و دوم یک واکنش تعادلی است که مقادیر بیشتری طلای محلول را به شکل یونهای کلوراترات ، AuCl4- (4) تولید می کند.
اکسیداسیون طلا توسط اسید نیتریک:
Au (s) + 3 NO3- (aq) + 6 H + (aq) → Au3 + (aq) + 3 NO2 (g) + 3 H2O (l)
انحلال طلا با تشکیل کلراورات:
Au3 + (aq) + 4 Cl- (aq) → AuCl4- (aq)
مشاهده فیلم زیر میتواند شما را در این باره کمک کند: